创新是中国医疗器械产业向高端发展的必由之路。未来,拥有自主创新能力、产品技术附加值高、具有差异化竞争优势的医疗器械企业有望快速成长。
2015年以来,我国多次颁布创新医疗器械相关文件,在监管和审批流程层面对创新医疗器械给予支持,其中国家药监局先后印发《创新医疗器械特别审查程序》、《医疗器械优先审批程序》,旨在创新产品和临床急需产品“单独排队,一路快跑”。
此外,国家医保局亦多次明确,“由于创新医疗器械临床使用尚未成熟、使用量暂时难以预估,尚难以实施带量方式。在集中带量采购之外留出一定市场为创新产品开拓市场提供空间”——这被业内看作是创新医疗器械暂不纳入集采的重要信号。
根据国家药监局医疗器械审评中心官网信息汇总整理,截至目前,经由创新医疗器械特别审查程序,倚锋已投企业旗下共有国内10款医疗器械进入创新审批绿色通道,其中4款产品已获批上市。
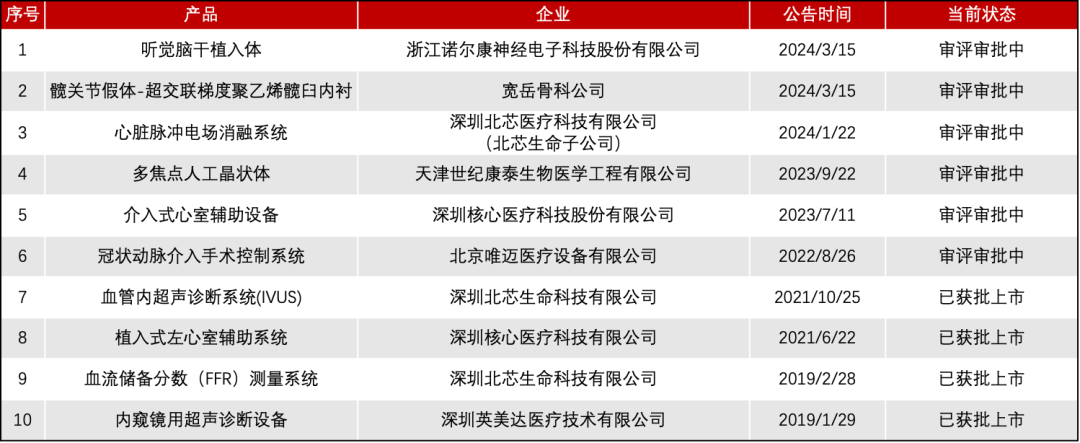
倚锋已投企业旗下进入创新审批绿色通道的医疗器械产品
“创新医疗器械特别审查程序”是国家药品监督管理局设立的快速审批通道,旨在鼓励医疗器械研发创新,促进医疗器械新技术的推广和应用,推动医疗器械产业高质量发展。
尤其是该制度2018年12月修订实施后,不仅要求申报产品必须是申请人主导的技术创新活动,在中国依法拥有产品核心技术发明专利权,且需完成前期临床研究,研究数据效果优良。
上述10款产品已进入创新国家药品监督管理局器械特别审查程序,意味着这些产品在科技水平、创新技术、使用性能都拥有领先地位,也直接证明了倚锋资本在高端医疗器械布局上的独到眼光。
不过,需要补充说明的是,进入创新审查程序不代表已认定产品具备可获准注册的安全有效性,申请人仍需按照有关要求开展研发及提出注册申请,药品监督管理部门及相关技术机构将按照早期介入、专人负责、科学审查的原则,在标准不降低、程序不减少的前提下进行审评审批。
以下是关于10款入选产品的详细信息:
1.诺尔康-听觉脑干植入体
诺尔康人工听觉脑干系统主要针对Michel畸形、初级听泡、耳蜗未发育等内耳畸形和蜗孔畸形、内听道狭窄、耳蜗/蜗神经发育不良等无法植入人工耳蜗或者植入人工耳蜗无效的患者,帮助他们绕过内耳和听神经,直接刺激脑干上耳蜗核使他们重回有声世界,这是国内首个脑干刺激产品。
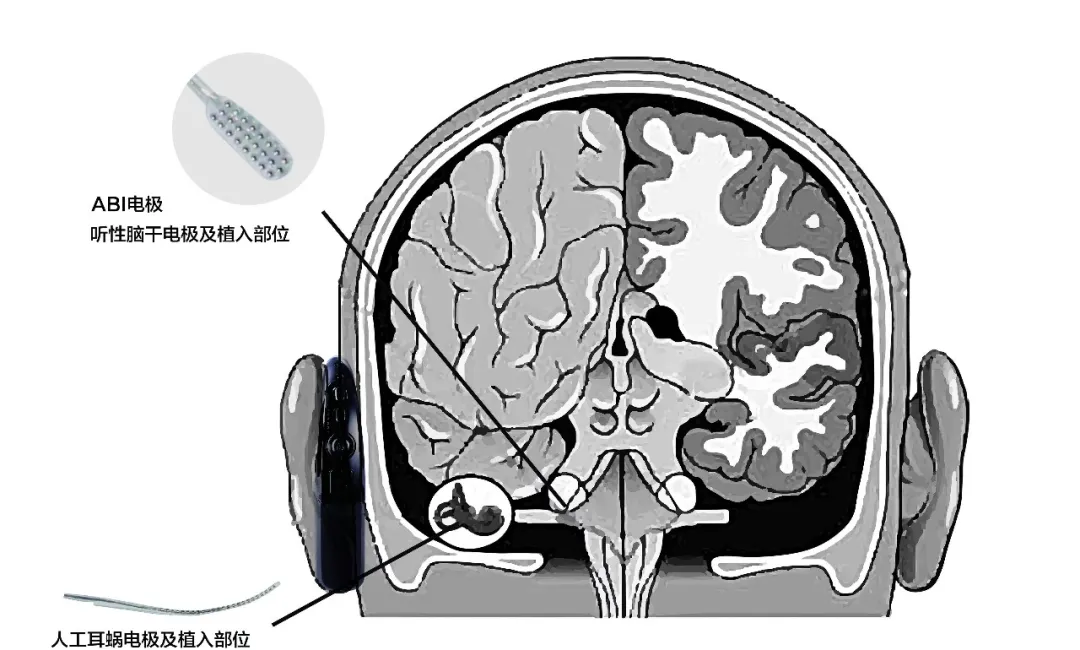
植入部位图解,来源《中国医疗器械信息》杂志
整个系统分为两部分,体内的听觉脑干植入体和体外的言语处理器。言语处理器将声音接收到后经过编码传给体内的植入体,植入体其电极须绕过受损的耳蜗、蜗神经,直接刺激脑干耳蜗核,产生听觉。
此次诺尔康WH-01A听觉脑干植入体作为国内第一个在脑干部位的刺激器进入国家药监局创新器械审查程序,标志我国将有望彻底解决感音神经性耳聋问题,突破国外中枢电子生物植入装置“卡脖子”难题,填补国内市场空白。
2.宽岳医疗-髋关节假体 超交联梯度聚乙烯髋臼内衬
该材料使用梯度交联技术,即在人工关节关键的摩擦界面表层上引入超高等效辐照交联度,从而实现更优的耐磨性;而随着材料深度增加交联度逐步下降,维持材料的机械韧度和强度。
研究证明该材料的清水磨损性能高于多款高交联聚乙烯部件,与陶瓷部件的磨损数据接近,同时机械韧性优于陶瓷,令设计和制造超薄、超耐磨的新型人工关节假体成为可能。
3.北芯生命-心脏脉冲电场消融系统
脉冲电场消融(PFA)技术是一种新型的具有组织选择性的非热效应电场技术,可在消融导管周围产生短时间高压电击使靶细胞膜上形成微孔,通过不可逆的电穿孔诱导细胞死亡。相较于传统消融方法,PFA操作时间更短,能瞬时完成对靶细胞持久性损伤,治疗后房颤复发率低。
PFA技术对参数和电极形态具有高度定制化要求,北芯的PFA系统由具有自主知识产权的InRythmTM心脏脉冲电场消融仪和LotosPFATM脉冲电场消融导管组成,采用目前全球最新的纳秒脉冲电场消融(nsPFA)技术,能进一步降低消融过程中的肌肉收缩,能够实现在局部麻醉下进行房颤消融,有效降低肺静脉狭窄、膈神经损伤或心房食管瘘等并发症的发生概率。
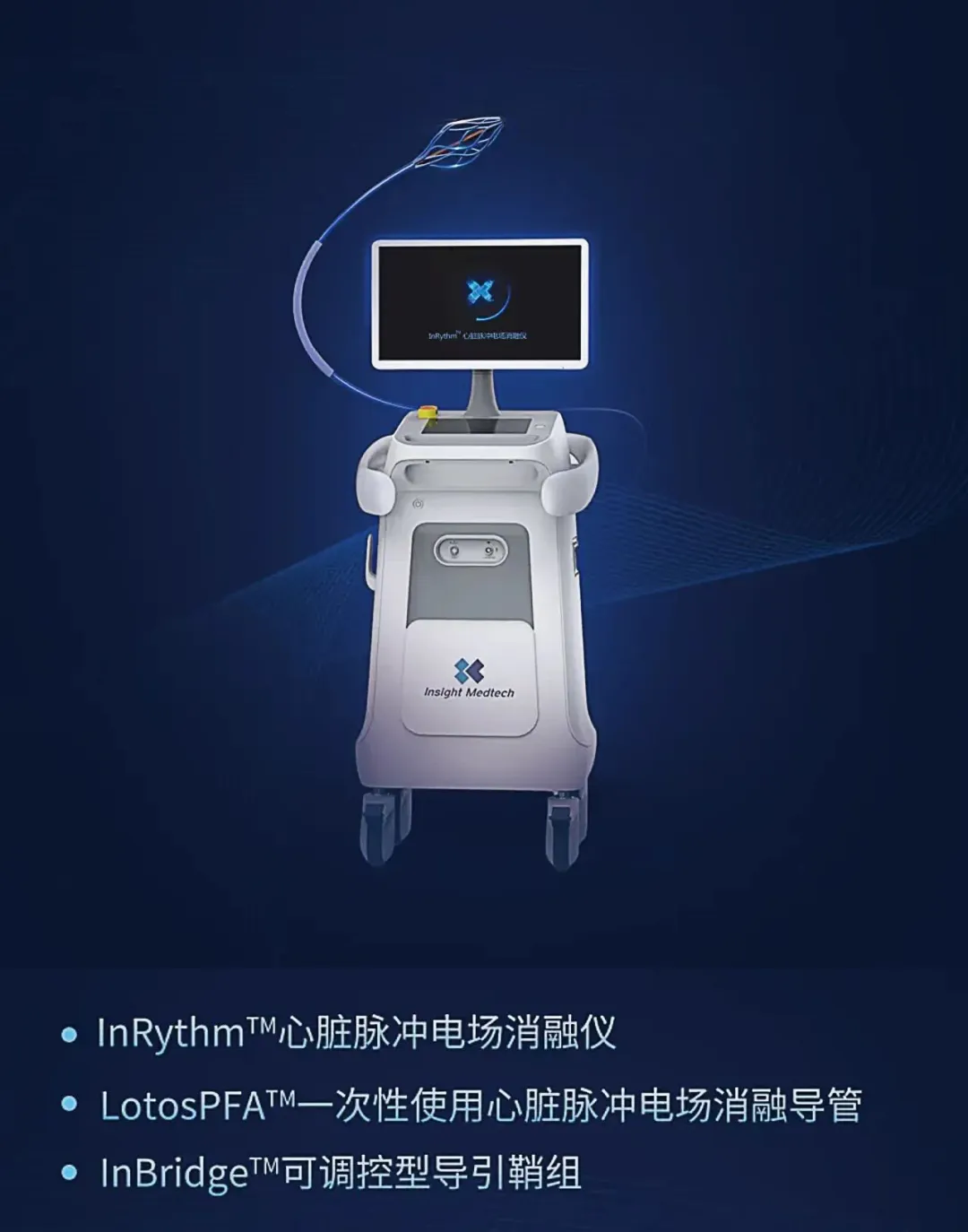
其中LotosPFATM脉冲电场消融导管具有针对PFA技术高度定制化创新设计的独特高密度电极和高稳定性的耦合式网篮设计,能够顺畅地到达并紧密贴合所有目标肺静脉,且在所有目标肺静脉位置均不易出现电极变形的情况,操作流程简单、能缩短术者的学习曲线,具备革新性的临床应用潜力。
4.世纪康泰-多焦点人工晶状体
“多焦点人工晶状体”是世纪康泰全球化战略中的核心产品之一,该产品提出一种全新的“非对称设计”,不仅将有效的用于成像的能量集中在远距、中距以及近距位置,同时,通过特殊的设计,将衍射能量分布在中距和近距之间,大幅度的减少这一视距范围的视觉断点,满足人们对远、中、近视力的迫切要求。

此外,该产品由中国专家针对中国人眼球参数和用眼习惯特别设计,首款国产60cm中距离设计,实现看电脑、手机,烹饪,阅读等场景舒适自如的连续视力,更符合中国人的用眼习惯。
5.核心医疗-介入式心室辅助设备
核心医疗旗下介入式心室辅助设备(pVAD),名为“CorVad® 介入式心室辅助系统”,是核心医疗自主研发、具有核心技术专利的新一代介入式人工心脏,该产品打破了国外技术垄断,实现了在极小的介入尺寸内产生超越同类产品的流量。

CorVad介入式心室辅助系统
同时CorVad还搭载了核心医疗自主设计的微型电机以及控制技术,能够有效降低溶血风险,进一步提升产品稳定性和长期运行可靠性。
目前该产品正在全国多家医院开展高危PCI和心源性休克临床研究,进一步验证其安全性和有效性。与此同时,核心医疗正在为CorVad研制更多的型号,为不同流量需求、不同支持时间需求的高危临床患者,提供满足中短期循环辅助的全方位治疗解决方案。
6.唯迈医疗-冠状动脉介入手术控制系统
唯迈医疗冠状动脉介入手术控制系统(ETcath),实现了高精度导管导丝智能仿生学推送、导丝智能触觉感知、多类型导管控制、3s无菌盒快拆等血管介入手术机器人的关键技术突破。
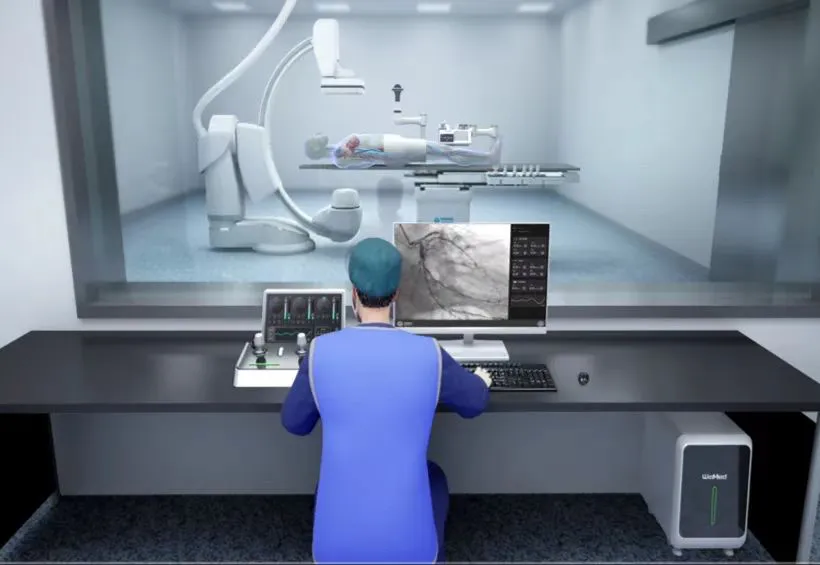
模拟操作示意图
手术过程中,由医生在监控室操作端操纵手柄,ETcath手术控制系统在手术室精确地实施对患者的PCI(经皮冠状动脉介入治疗)手术。
与传统介入手术相比,在上述产品辅助下,介入医生无需再穿着20斤左右的铅衣在X射线环境下做手术,而是可以坐在操控室控制机器人完成手术,控制精度和标准化也进一步提升,减少手术并发症。此外,该系统还能将操作手法数据化处理,进行术后回顾,通过大数据形成统一手术方案,进一步降低手术风险。
7.北芯生命-血管内超声诊断系统(IVUS)
北芯生命血管内超声(IVUS)诊断系统是中国首个自主创新60MHz高清高速国产IVUS产品,是北芯生命血管内影像学产品线的代表产品。
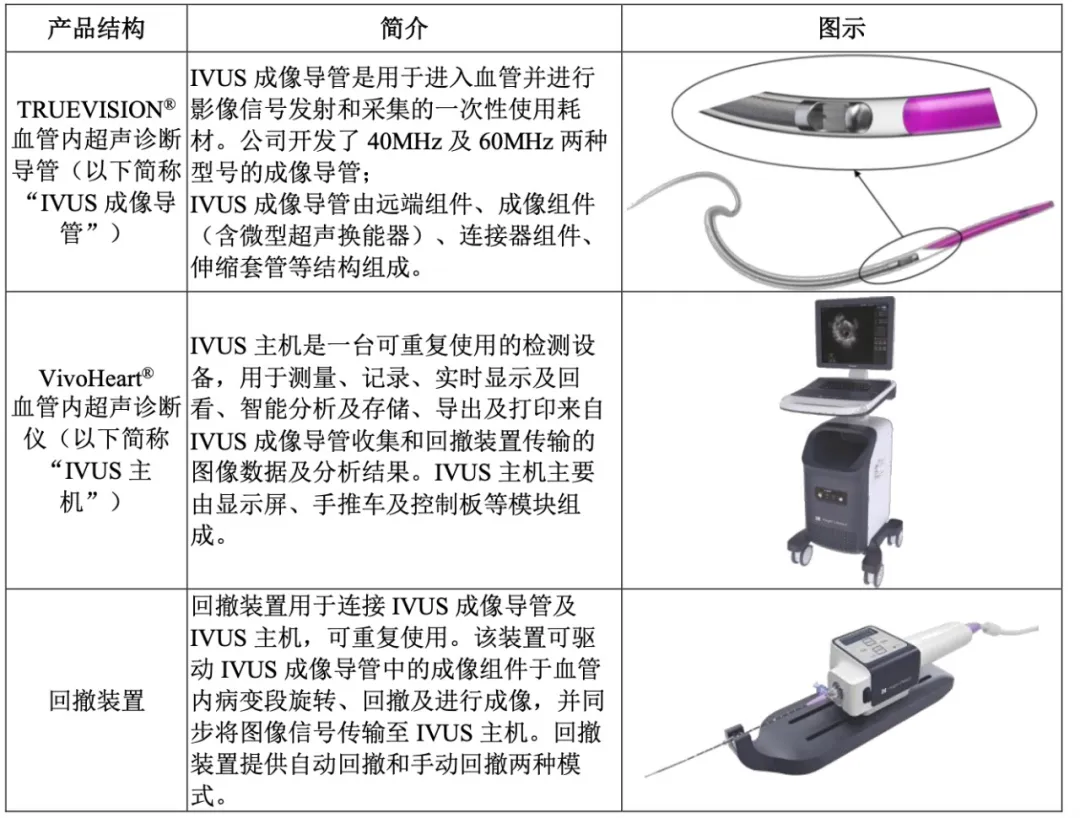
北芯生命IVUS系统结构概况
北芯生命完全自主研发整套IVUS系统,并且实现了高频微型超声换能器的国产技术突破,采用特有新型高速三维机械扫描及高频超声成像、高性能图像后处理等技术,拥有高清、高速、智能三大特点及业内最快的成像速度。
北芯生命于2018年8月承担国家科技部国家重点研发计划数字诊疗装备研发重点专项 “高分辨、高速、智能化心脏介入血管内超声成像系统”,IVUS系统进一步于2021年11月获批进入国家药监局创新医疗器械特别审查程序,并于2022年7月获批国家药监局第三类医疗器械注册证,并实现国内销售。
8.核心医疗-植入式左心室辅助系统
核心医疗植入式左心室辅助系统(俗称“人工心脏”)为第三代非接触式磁悬浮离心泵,核心技术主要为盘式电机技术,其利用位置传感器检测并控制转子的转速和悬浮高度。
该产品电机仅采用一组定子线圈同时控制转子的旋转和悬浮,结构更简单、重量更轻、体积更小、功耗更低,在临床应用中,手术切口较小,患者恢复较快,适用人群更广,并可降低血泵热量导致的血栓风险。
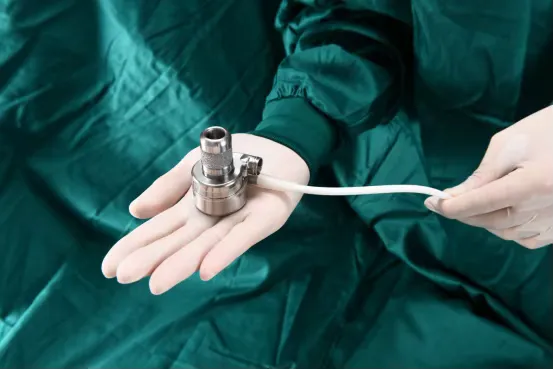
Corheart 6植入式左心室辅助装置
产品于2021年6月获批进入国家药监局创新医疗器械特别审查程序,并于2023年6月正式获得国家药品监督管理局(NMPA)批准上市,注册证编号为国械注准20233120716,成为新一代小型化全磁悬浮人工心脏的代表。
同时,这是一枚拥有完备自主知识产权的国产人工心脏,也是目前国内植入数量最多,全球体积最小、重量最轻的人工心脏,其血泵直径仅34毫米、厚度26毫米、重量约90克,比市场上同类产品直径缩小40%,重量减轻50%。
9.北芯生命-血流储备分数(FFR)测量系统
北芯生命FFR系统通过直接测量FFR使医生可对冠状动脉疾病患者的心肌缺血程度进行精准诊断,定位导致患者缺血的狭窄病变位置,指导后续PCI治疗策略及进行术后疗效评估,是公司血管内功能学产品线的代表产品。
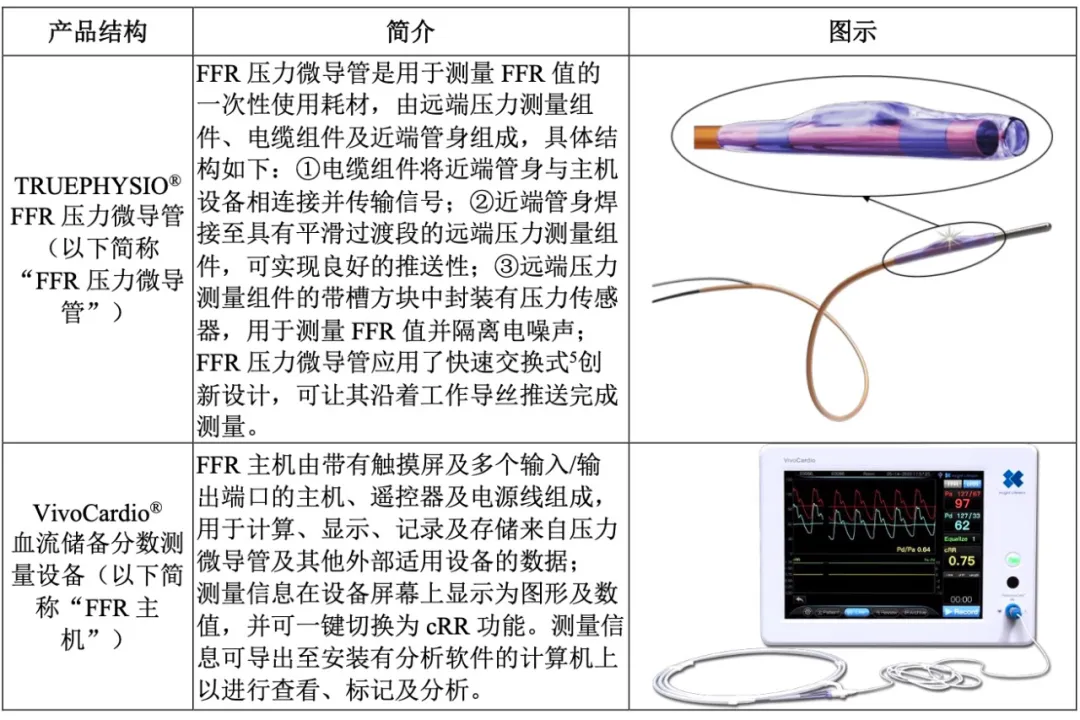
北芯生命FFR系统结构概况
上述产品于2019年2月获批进入国家创新医疗器械特别审查程序,于2020年3月取得CE认证并进入海外市场,于2020年9月获批国家药监局第三类医疗器械注册证并实现国内销售,为金标准FFR领域内中国首个获国家药监局批准的国产产品。
同时,其也是全球第一个将MEMS压力传感器封装至快速交换式微导管上的直接测量FFR产品,由公司自主设计及研发整套FFR系统,掌握包括传感器焊接、封装等核心技术的全部知识产权。
10.英美达医疗-内窥镜用超声诊断设备
英美达内窥镜用超声诊断设备由主机、探头驱动器、超声小探头、脚踏开关、台车组成,与上消化道内窥镜联合,用于对上消化道进行超声诊断检查。

在常规内窥镜直接观察消化道粘膜表面的病变基础上,该产品利用超声探头可以对病变粘膜下组织进行超声扫描观察,增强常规内镜检查的诊断效果,从而得到人体消化道壁的表层图像和周围器官的断层图像等多元信息。
该产品于2019年1月进入国家创新特别审批医疗器械审查程序,于2020年7月完成临床试验,2021年9月获药监局批准上市。
该设备也是首个国产内窥镜超声诊断设备,产品采用自主开发的高频超声硬件、微型成像探头以及高性能软件构架和图像处理新技术,可以极大地提升内窥镜下超声影像质量,有助于发现早期消化道肿瘤,提高患者的生存率。